
英文标题:Insulin Resistance Compromises the Pentose Phosphate Pathway and Impairs Left Ventricular Assist Device–Mediated Myocardial Recovery in Obese Patients with Heart Failure
中文标题:胰岛素抵抗损害磷酸戊糖途径并损害肥胖心力衰竭患者左心室辅助装置介导的心肌恢复
发表期刊:Circulation
影响因子:38.7
合作单位:上海交通大学医学院附属上海儿童医学中心
百趣提供服务:非靶代谢流、靶标代谢流
研究背景
心力衰竭(Heart failure, HF)是全球范围内的重大健康危机,影响数百万人群,死亡率居高不下,给医疗系统带来沉重负担。近些年,左心室辅助装置(LVAD)作为机械循环支持的核心技术,已从“移植桥梁”逐步发展为“恢复桥梁”,通过机械卸载减轻心室负荷、促进逆重构,部分患者可实现装置移除,成为终末期HF患者的重要治疗选择。然而,临床实践中发现,并非所有患者都能在LVAD支持下实现心肌恢复:部分患者心功能显著改善,而另一部分患者则难以获益,其潜在机制尚未得到系统阐明。基于此,本研究通过临床数据分析、动物模型模拟及多组学技术,探究胰岛素抵抗、磷酸戊糖途径(PPP)与LVAD介导心肌恢复的关联,为优化肥胖HF患者的LVAD治疗策略提供理论依据。
研究结论
01.肥胖HF患者的LVAD介导心肌恢复因胰岛素抵抗而减弱
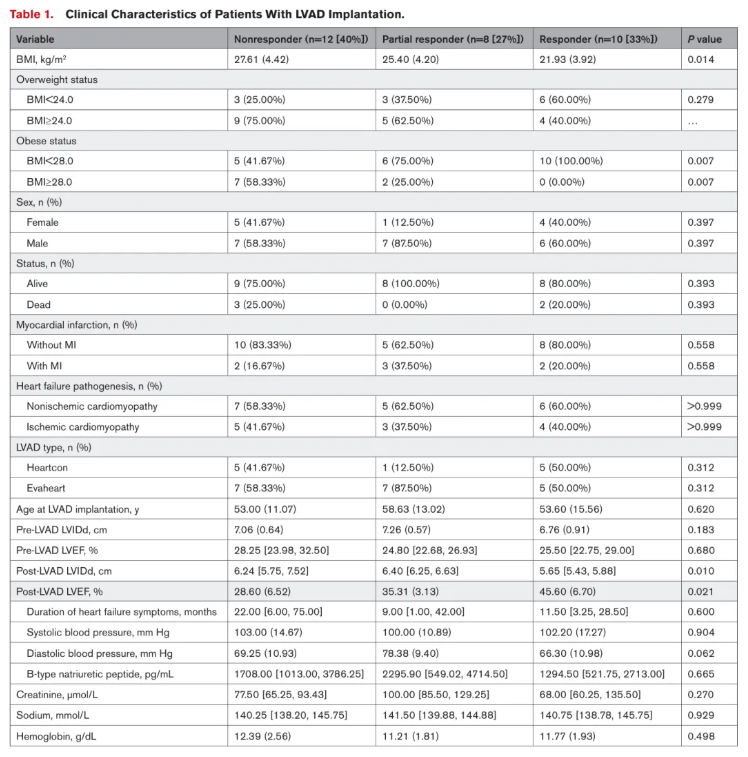
研究纳入6个医疗中心30例LVAD植入患者,按心肌恢复程度分为三组。研究结果显示,体重指数(BMI)及肥胖患者(BMI≥28.0)的比例在三组间差异显著(表1),其他临床特征无明显不同,这表明肥胖与患者心肌恢复程度之间存在显著关联。
表1 LVAD植入患者的临床特征
安装IVAD后6个月,非肥胖组左心室舒张末期内径(LVIDd)显著降低、左心室射血分数(LVEF)显著升高(图1A-B),实现心肌恢复;而肥胖组这两项指标无显著变化(图1C-D),说明肥胖患者LVAD介导的心肌恢复受抑。进一步分析发现,肥胖组的胰岛素抵抗指数(HOMA-IR)显著高于非肥胖组(图1E);散点图显示,无应答者集中在高BMI、高胰岛素抵抗象限,应答者则在低水平象限(图1F),且无应答者HOMA-IR水平最高(图1G),其与心功能改善程度呈负相关(图1H-I)。此外,单细胞RNA测序(snRNA-seq)显示,无应答者心肌细胞的胰岛素受体(INSR)、IRS2表达更低,且存在胰岛素抵抗相关转录特征—胰岛素抵抗通路上调,胰岛素信号及PI3K-Akt通路下调。由此可见,肥胖诱导的胰岛素抵抗是人类LVAD介导心肌恢复不佳的关键因素。
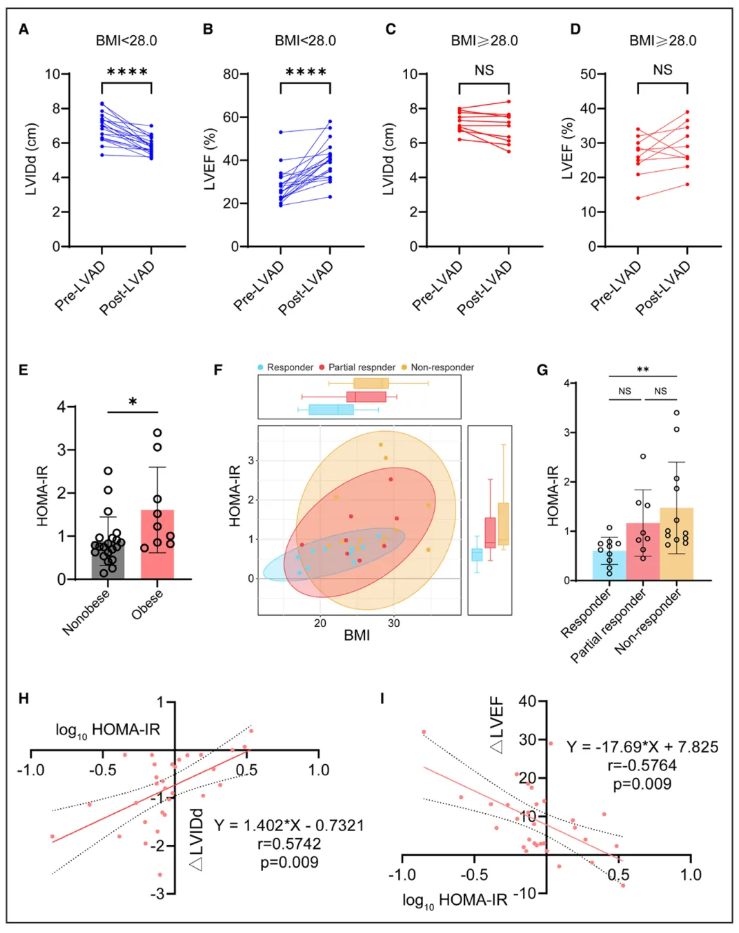
图1 胰岛素抵抗与肥胖HF患者LVAD介导的心肌恢复有关
02.心肌INSR信号通路与葡萄糖摄取在卸载心脏中上调
为探究上述结果的潜在机制,研究采用同系异位颈部心脏移植小鼠模型模拟LVAD卸载。首先,通过snRNA-seq探索了心脏卸载中涉及的信号通路(图2A),识别出11个基于经典标志物的细胞亚群(图2B)。与负荷心脏相比,卸载心脏的细胞类型组成显著不同(图2C),差异基因富集于代谢通路(图2D),其中心肌细胞的代谢评分最高(图2E)。进一步分析显示,卸载心脏的心肌细胞脂肪酸氧化相关基因表达降低,INSR及葡萄糖摄取相关基因表达升高;胰岛素信号通路、PI3K-Akt通路富集(图2G-H),这些通路相关基因在蛋白互作网络中处于核心位置,且在卸载心肌细胞中转录水平更高(图2I-J)。
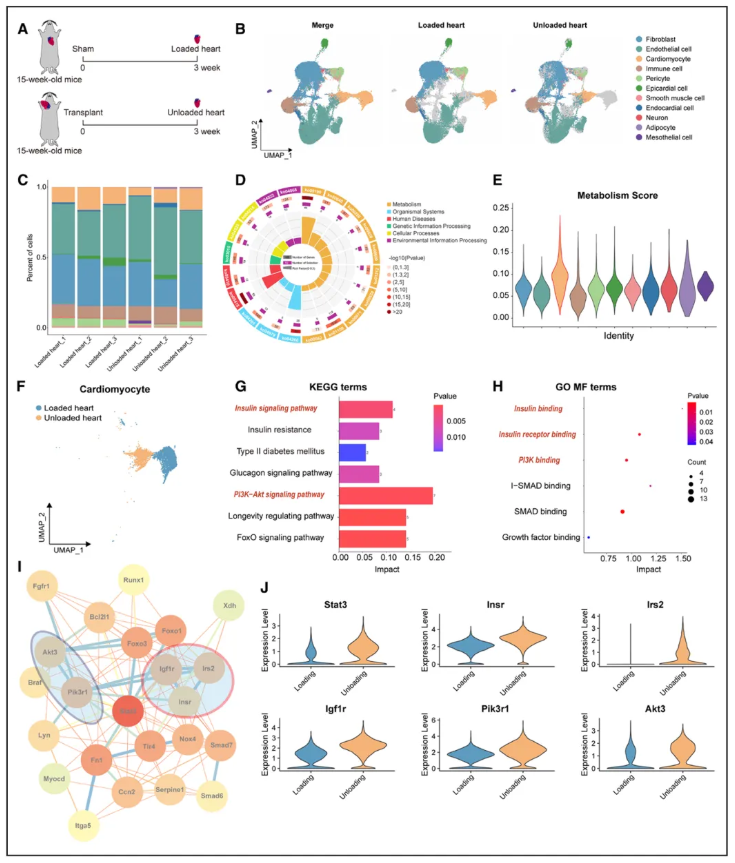
图2 卸载心脏中的胰岛素受体信号通路活性和葡萄糖摄取高于负荷心脏
蛋白印迹(WB)与影像学分析验证上述发现:卸载心脏中INSR与PI3K-Akt通路磷酸化水平、GLUT4蛋白表达(图3A-C)及心肌葡萄糖摄取(图3D-E)均显著升高,而脂肪酸氧化关键蛋白表达下降(图3F)。为明确INSR的关键作用,研究通过AAV9介导的局部基因敲低技术,特异性敲低卸载心肌中的Insr表达(图3G-H)。结果显示,敲低卸载心脏中的Insr后,下游IRS2/PI3K-Akt通路磷酸化、GLUT4表达及葡萄糖摄取均显著降低(图3I-K),同时脂肪酸氧化蛋白表达回升(图3L),证实INSR激活是卸载诱导心肌葡萄糖摄取增加的核心原因。
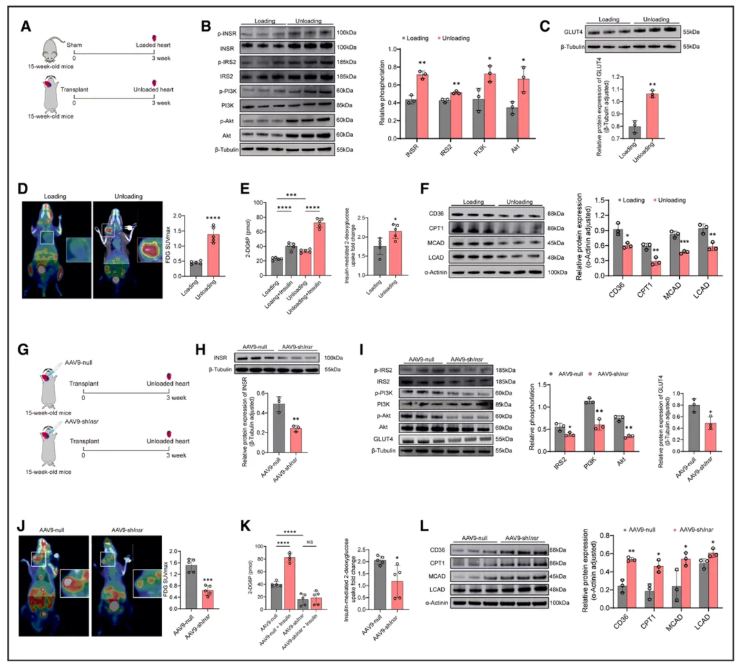
图3 INSR在卸载心脏葡萄糖摄取的上调中起重要作用
03.卸载状态下心肌磷酸戊糖途径上调
如图4所示,研究以[U-¹³C]葡萄糖示踪非靶标代谢组学探究卸载心脏的代谢转向,其中卸载与负荷心脏的¹³C标记葡萄糖代谢存在显著差异(图4B)。差异丰度评分分析表明,仅中心碳代谢在卸载状态下上调(图4C),且¹³C标记差异代谢物主要集中于PPP(图4D);计算标记代谢物占总通量的比例发现,PPP相关代谢物上调、糖酵解无差异、三羧酸循环下调(图4E)。因此,卸载心脏的葡萄糖主要流向PPP。
snRNA-seq验证显示,卸载状态下心肌细胞的葡萄糖摄取及PPP相关基因上调,三羧酸循环基因下调(图4F)。结合[1,2-¹³C]葡萄糖示踪靶标代谢组学,卸载心脏的PPP相关代谢物同位素含量升高(图4H),(m+2)和(m+1)标记的PPP衍生代谢物比例显著高于负荷心脏(图4I),且NADPH/NADP⁺比值升高(图4J)。此外,[U-¹³C]棕榈酸示踪显示,卸载心脏的TCA循环中脂肪酸衍生标记中间体减少,亦暗示着脂肪酸氧化受抑。综合来看,机械卸载可重编程心肌代谢,使得葡萄糖代谢转向PPP,同时抑制脂肪酸氧化。
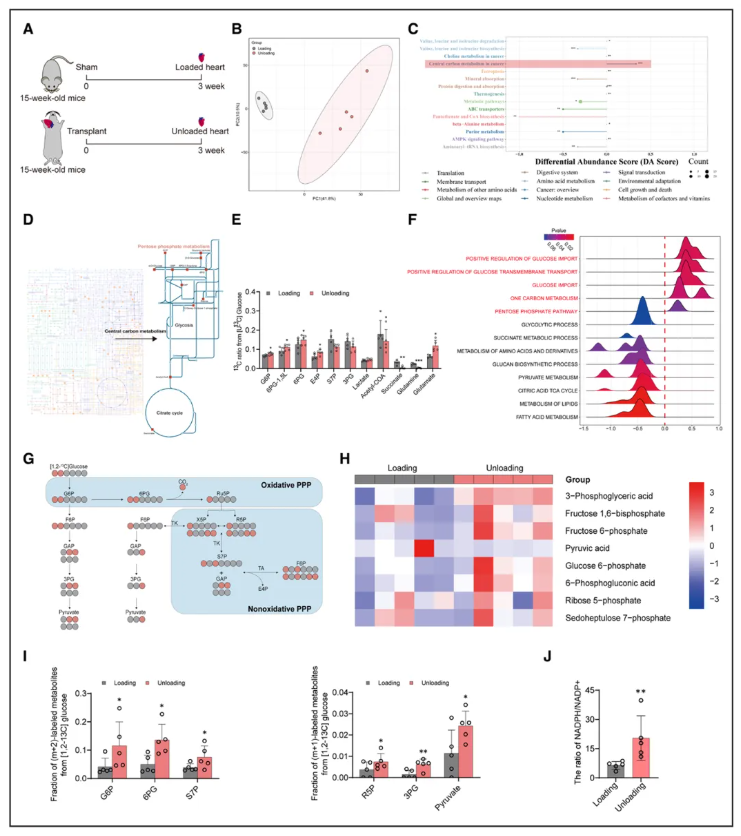
图4 卸载心脏摄取的葡萄糖主要进入磷酸戊糖途径(PPP)以产生NADPH
04.心脏卸载通过PPP修复衰竭心脏
基于冠脉结扎心衰模型,研究移植构建出心脏卸载模型,用以明确心脏卸载对心衰心肌恢复的影响及PPP的介导作用。组内对比显示:与负荷组相比,卸载组3周时的心功能指标均得到显著改善,即心功能在卸载后得到恢复。病理检测显示,心脏卸载后,其心肌细胞凋亡减少(图5B)、梗死区纤维化减轻(图5C)、Ⅰ/Ⅲ型胶原比例降低(图5D)、心肌肥大逆转(图5E)。分子层面,卸载组的葡萄糖摄取(图5F)、INSR-PI3K-Akt通路活性及GLUT4表达(图5G-H)均显著升高。更重要的是,PPP关键酶(TKT、TALDO1、G6PD)表达及NADPH/NADP⁺比值上调(图5I-J),同时氧化应激标志物减少,抗氧化酶SOD2表达增加(图5K-L),线粒体呼吸功能在卸载后也得到改善(图5M),表明PPP上调通过增加NADPH生产,减轻了心肌氧化应激。
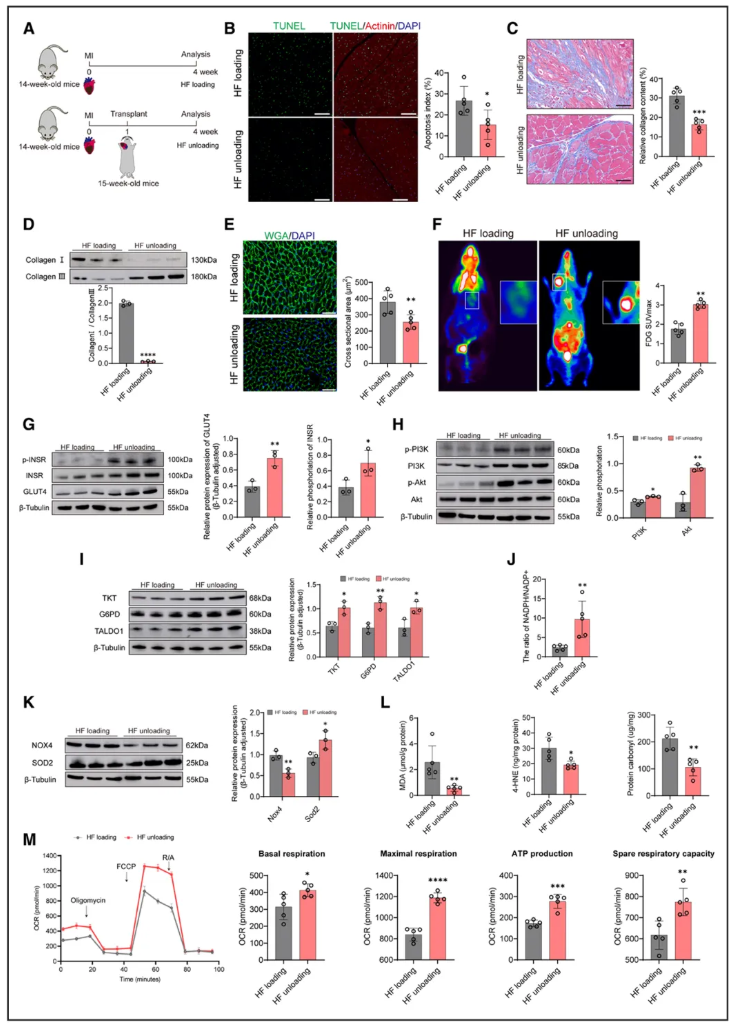
图5 卸载通过磷酸戊糖途径减轻衰竭心脏的氧化应激
结合关键敲低实验,亦证实PPP是该修复机制的关键介导之一:当敲低PPP关键酶G6pd(图6A-B)后,NADPH生成减少(图6C),氧化应激增强(图6D-E),线粒体功能受损(图6F),心肌凋亡与纤维化加重(图6G-I),心功能恢复受阻(图6J-K)。
综上所述,心脏卸载通过激活INSR信号通路促进葡萄糖摄取,进而上调PPP活性,增加NADPH生成以减轻心肌氧化应激,最终实现衰竭心脏的结构与功能修复,其中INSR信号和PPP是该修复过程的核心介导因素。
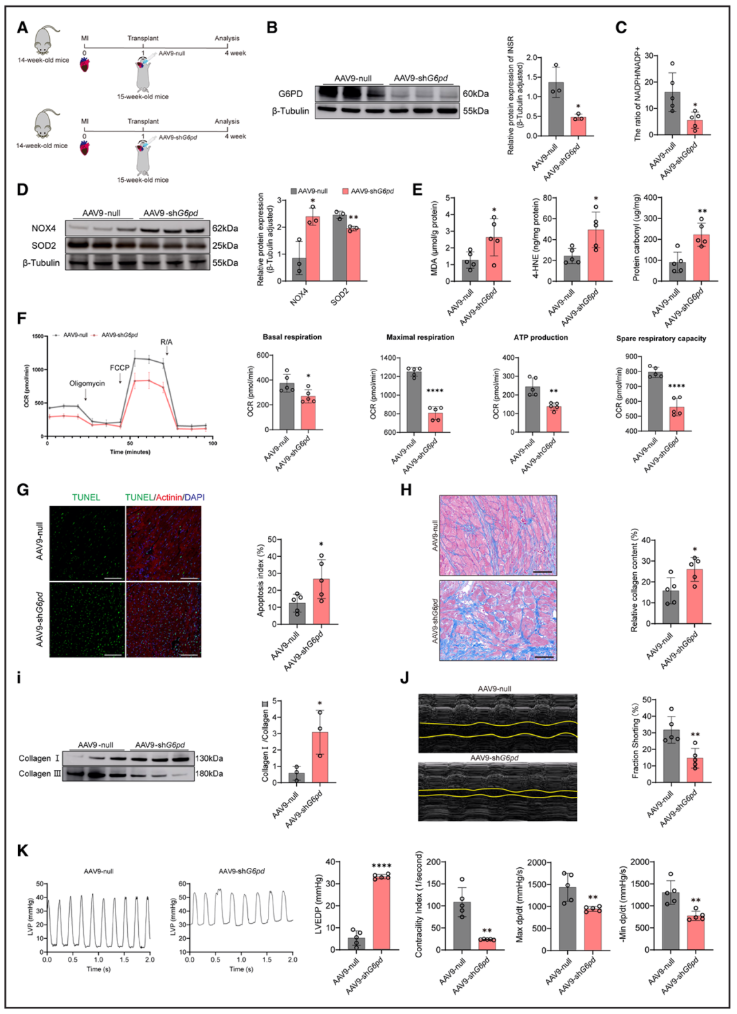
图6 抑制PPP减弱了卸载介导的衰竭心脏心肌恢复
05.胰岛素抵抗抑制PPP并减弱肥胖小鼠中卸载介导的心肌恢复
基于临床观察,本研究在肥胖小鼠中建立心衰及心脏移植模型,以验证肥胖相关的胰岛素抵抗是否削弱卸载介导的心肌恢复。在此模型中,高脂饮食诱导的肥胖小鼠表现出胰岛素抵抗。与正常小鼠模型不同,肥胖小鼠的衰竭心脏在卸载后并未出现心功能指标的显著改善,表明恢复过程依旧受损。组织学分析显示,卸载组与负荷组在心肌细胞凋亡(图7B)、心肌纤维化(图7C)及胶原蛋白比例(图7D)均无显著差异。分子层面,在肥胖背景下,卸载并未有效激活INSR-PI3K-Akt信号通路及GLUT4表达(图7F-G),心脏葡萄糖摄取无增加(图7E),PPP关键酶表达及NADPH/NADP⁺比值亦未上调(图7H-I)。此外,心脏氧化应激水平(图7J-K)与线粒体呼吸功能(图7L)也未改善,说明代谢-抗氧化轴激活失败。然而,过表达G6PD后,肥胖小鼠卸载心脏的心功能却显著恢复,揭示靶向激活PPP可以挽救恢复障碍。简言之,肥胖诱导的胰岛素抵抗确实能够削弱卸载介导的心肌恢复,其核心机制是通过抑制心肌葡萄糖的摄取及其PPP活性。
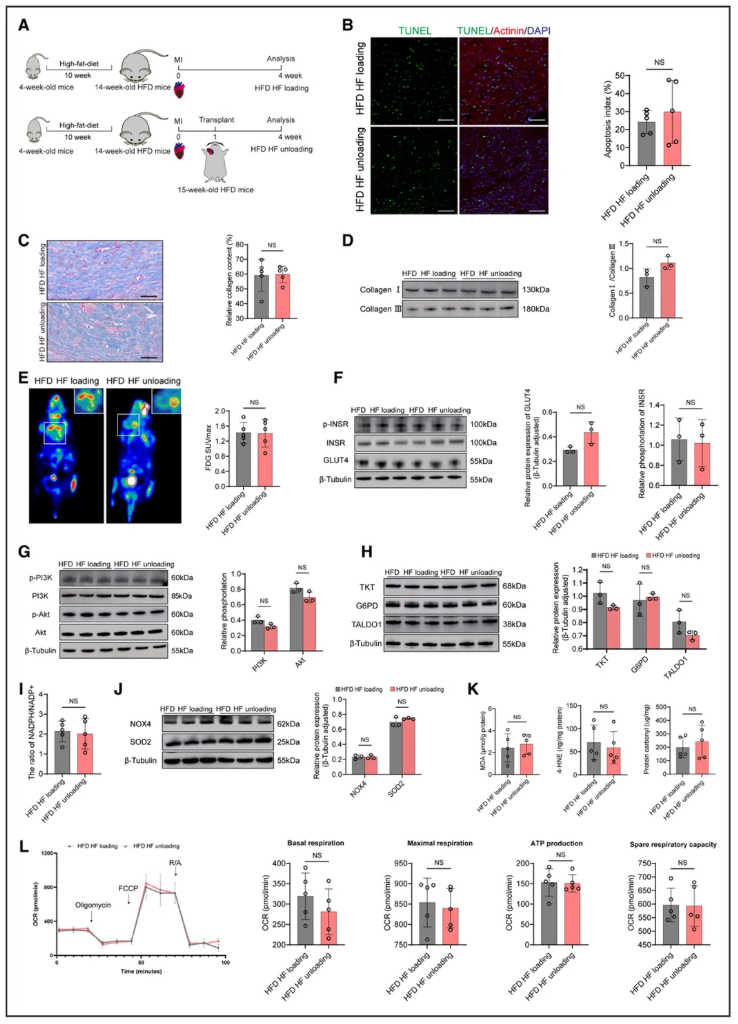
图7 肥胖通过抑制PPP来阻碍卸载介导的心肌恢复
06.吡格列酮恢复肥胖小鼠卸载介导的心肌恢复
基于胰岛素抵抗抑制心肌恢复的发现,本研究欲进一步探究改善胰岛素敏感性能否恢复卸载的有益作用。为此,研究聚焦胰岛素增敏剂“吡格列酮(Pioglitazone)”,对接受心脏移植的肥胖小鼠进行了为期3周的药物治疗。结果而言,该治疗显著改善了小鼠的葡萄糖耐量与胰岛素敏感性,同时恢复了卸载介导的心肌恢复。在病理上,治疗组的心肌细胞凋亡(图8D)、梗死区纤维化(图8E)、Ⅰ/Ⅲ型胶原比例(图8F)等均得到有效改善。
在分子与代谢方面,吡格列酮不仅增强了卸载衰竭心脏的葡萄糖摄取(图8G),而且上调了PI3K-Akt与INSR通路的磷酸化水平以及GLUT4的表达(图8H-I)。同时,PPP关键酶(G6PD、TKT、TALDO1)的表达及NADPH/NADP⁺比值也显著上升(图8J-K)。伴随着PPP的激活,心脏氧化应激减轻(图8L-M),线粒体呼吸功能得到改善(图8N)。总体而言,吡格列酮复原了肥胖HF小鼠的卸载介导心肌恢复,有效证实了胰岛素增敏剂类药物所具有的治疗潜力,而其效用是通过改善胰岛素敏感性,激活INSR-PI3K-Akt通路,上调PPP介导的氧化还原稳态所实现。
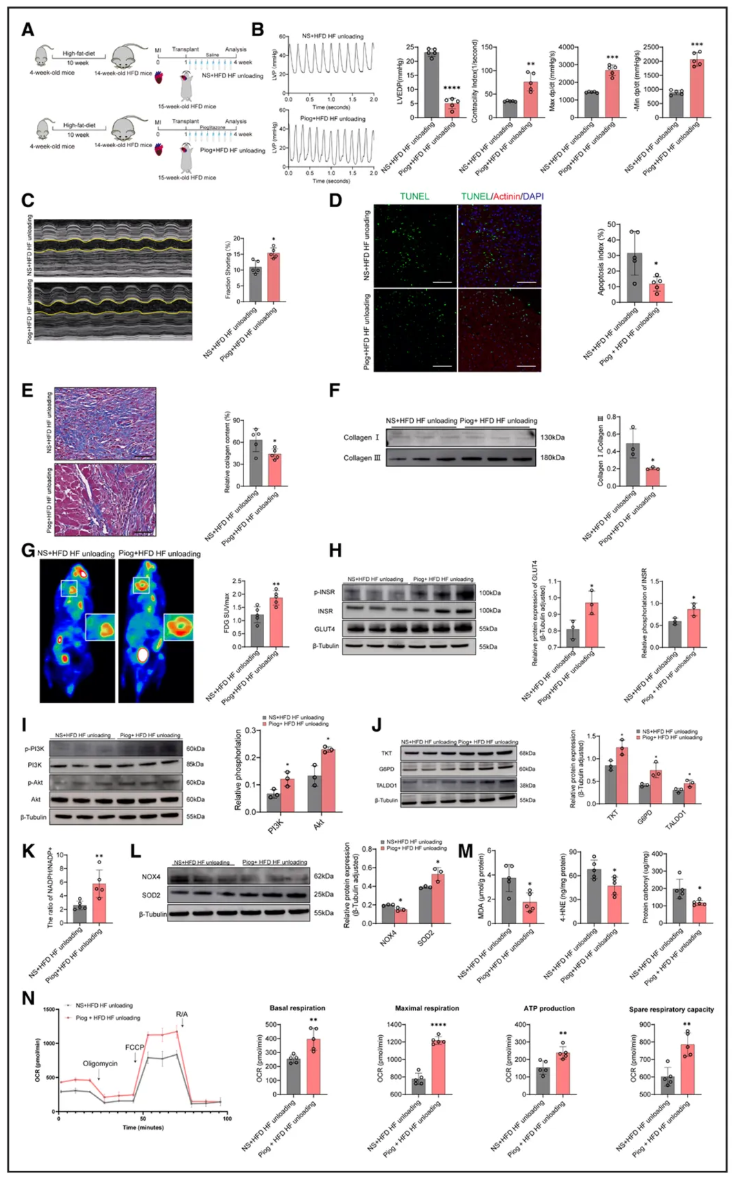
图8 吡格列酮可恢复肥胖小鼠中卸载介导的心肌恢复
研究总结
本研究聚焦终末期心力衰竭(HF)患者LVAD介导的心肌恢复差异问题,通过临床数据分析、小鼠异位心脏移植模型构建及单细胞RNA测序、稳定同位素示踪代谢组学等多技术手段,系统探究了肥胖相关胰岛素抵抗的影响及分子机制。研究发现,BMI≥28.0的肥胖HF患者因胰岛素抵抗,LVAD介导的心肌恢复显著受损;机制上,机械卸载通过YAP-TEAD4通路激活心肌INSR信号,促进葡萄糖摄取并转向PPP,生成NADPH以减轻氧化应激,而PI3K-Akt-MDM2通路通过稳定G6PD进一步强化该保护效应;肥胖诱导的胰岛素抵抗会阻断这一代谢重编程过程,而吡格列酮等胰岛素增敏剂可恢复INSR-PPP轴功能,逆转心肌恢复障碍。该研究揭示了胰岛素抵抗-PPP轴在LVAD疗效中的核心作用,为肥胖HF患者制定个性化代谢干预策略、提升LVAD治疗获益提供了重要理论依据。