
文章标题:Integrated Proteomic and Metabolomic Profiling for Developing Novel Plasma-Based Diagnostic Models of Sarcopenia
发表期刊:Journal of Cachexia, Sarcopenia and Muscle
影响因子:9.1
客户单位:四川大学华西医院
百趣提供服务:新一代代谢组学NGM 2
研究背景
肌少症是与年龄相关的进行性骨骼肌疾病,以骨骼肌质量、力量和运动能力下降为核心特征。60岁以上人群患病率达10%~20%,80岁以上超30%,易引发跌倒、骨折等不良事件,显著加重医疗负担,早期诊断对延缓病情进展至关重要。当前临床诊断金标准依赖专业设备与耗时检测,可扩展性差,难以开展大规模人群筛查;现有血浆生物标志物诊断准确性欠佳,灵敏度和特异性鲜有超过80%。高通量组学技术为解析疾病复杂机制、挖掘可靠生物标志物提供了新手段:Olink蛋白组学可实现低丰度蛋白的精准定量,LC MS非靶标代谢组学能够全面解析代谢紊乱特征。多组学整合已在多种疾病诊断中展现出协同优势,但针对肌少症的诊断应用研究仍十分有限。本研究针对上述临床痛点,拟整合Olink蛋白组与非靶标代谢组技术,结合机器学习构建高性能肌少症血浆诊断模型,为开发无创、可规模化推广的临床筛查工具奠定基础。
研究结果
01.参与者特征
为明确研究纳入受试者的基线特征,验证病例-对照分层的有效性,本研究对发现队列(40例肌少症/40例非肌少症)和验证队列(30例肌少症/30例非肌少症)共140名受试者的人口学特征、体测指标及合并症情况进行统计分析(图1)。
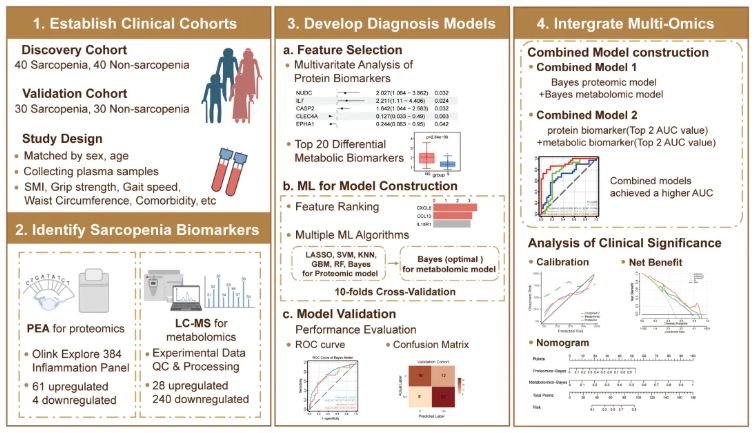
图1. 研究流程示意图
结果显示,发现队列中肌少症组与非肌少症组中位年龄分别为72.00岁、71.50岁,验证队列中分别为71.00岁、71.50岁,两组年龄比较均无统计学差异;发现队列两组女性占比均为52.50%,验证队列均为53.33%,性别分布无显著差异;高血压、冠心病、脑卒中、糖尿病等年龄相关合并症的患病率在两组间也均无统计学差异,提示队列年龄、性别匹配均衡。肌少症组的骨骼肌质量指数(SMI)、握力、步速在两个队列中均显著低于非肌少症组,小腿围、中上臂围、腰围、臀围等体测指标亦显著降低,肱三头肌皮褶厚度在发现队列中也显著低于非肌少症组。上述结果表明,本研究肌少症组受试者均符合2019 AWGS肌少症诊断标准,病例-对照分层有效、基线匹配均衡,可排除年龄、性别及常见合并症对后续组学与模型分析的干扰(图2)。
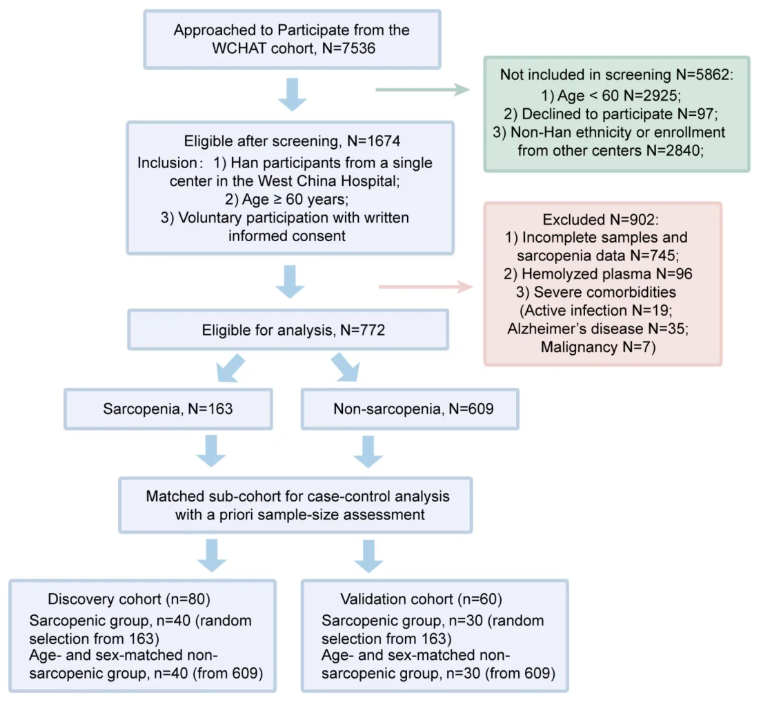
图2. 受试者招募流程图
02.蛋白质组学分析揭示肌少症相关炎症特征
为探究肌少症相关的血浆炎症蛋白表达特征并构建蛋白组学诊断模型,本研究采用Olink Explore 384炎症Panel对研究队列血浆样本进行蛋白质组学检测。结果显示,主成分分析表明肌少症组与非肌少症组的蛋白表达谱呈现明显聚类分离(图3A);研究共鉴定出65种差异表达蛋白,其中61种上调、4种下调(图3B-C)。GO功能富集分析显示,差异蛋白显著富集于RAS蛋白信号转导、小GTP酶介导信号转导及肽基-苏氨酸磷酸化等生物学过程(图3D);KEGG通路分析表明,FcγR介导的吞噬作用、趋化因子信号通路及NF-κB信号通路显著富集(图3E)。蛋白-蛋白互作网络分析进一步证实,差异蛋白主要参与趋化因子与细胞因子相互作用,明确炎症紊乱与肌少症发生密切相关(图3F)。
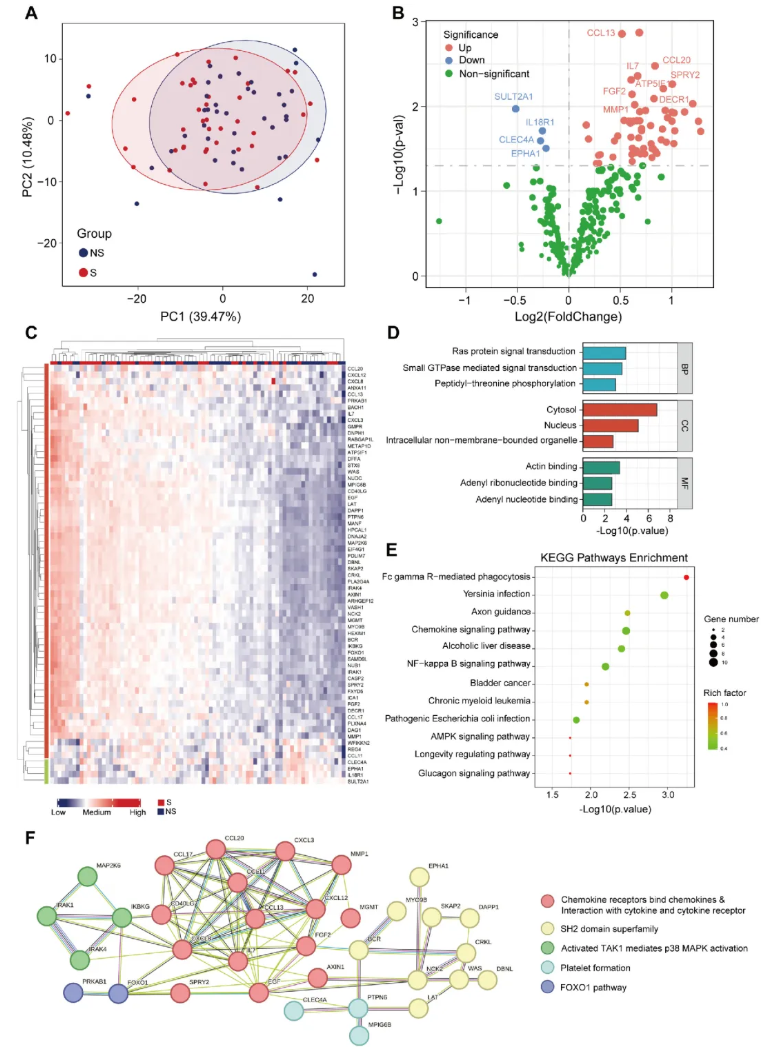
图3. 肌肉减少症的蛋白质组学特征及差异表达蛋白分析
为构建稳健的诊断模型,本研究采用多算法特征筛选结合10折交叉验证进行模型构建(图4A)。经年龄、性别、BMI等临床协变量校正后,筛选出24个肌少症相关蛋白标志物,并按变量重要性排序(图4B);随后构建6种机器学习诊断模型,其中高斯朴素贝叶斯模型表现最优,最终纳入7个核心蛋白,在发现队列AUC为0.743,验证队列AUC为0.698,验证队列灵敏度60.0%、特异度73.3%(图4C–E)。单标志物分析显示,CCL13与FGF2诊断效能最优,发现与验证队列AUC均在0.68–0.70之间,ELISA验证亦证实两组间表达差异显著;且多数差异蛋白与骨骼肌质量指数、握力等核心临床指标显著相关。
上述结果表明,肌少症患者存在明显的血浆炎症蛋白谱紊乱,本研究构建的七蛋白高斯朴素贝叶斯模型具有良好的肌少症诊断价值,CCL13和FGF2可作为潜在核心蛋白标志物,为后续多组学整合诊断模型构建奠定了蛋白组学基础。
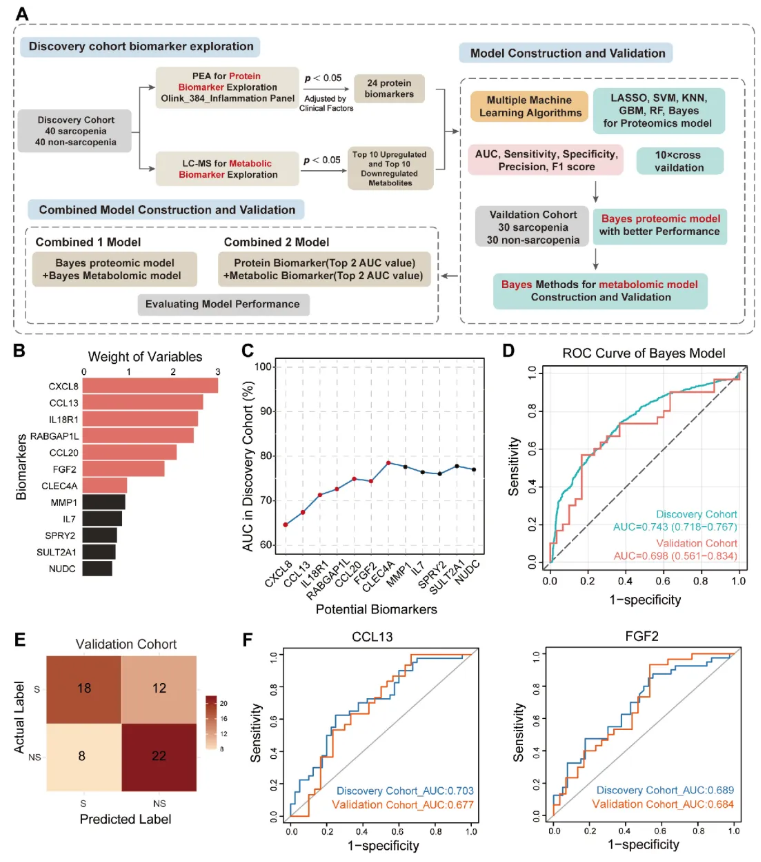
图4. 基于蛋白质组学的机器学习算法对肌少症(S)与非肌少症(NS)组的区分
03.肌少症患者的代谢组学分析
为探究肌少症相关的血浆代谢特征并构建代谢组学诊断模型,本研究采用LC-MS非靶标代谢组学对研究队列血浆样本进行检测,采用与蛋白质组学一致的高斯朴素贝叶斯算法进行标志物筛选与模型构建验证。结果显示,正交偏最小二乘判别分析(OPLS-DA)表明肌少症组与非肌少症组代谢谱呈显著分离(图5A);共鉴定出268种差异代谢物,其中28种上调、240种下调(图5B),差异表达前20种代谢物聚类热图可见组间清晰分离(图5C)。KEGG通路富集分析显示,差异代谢物显著富集于甘氨酸-丝氨酸-苏氨酸代谢、支链氨基酸生物合成、氨基酸生物合成通路,富集分数均>3,提示氨基酸代谢紊乱在肌少症中发挥关键作用。
经特征筛选与模型优化,按变量重要性对差异代谢物排序(图5D),最终纳入7种核心代谢物构建高斯朴素贝叶斯模型,为最优代谢组学诊断模型;该模型在发现队列AUC为0.828,验证队列AUC为0.751(图5E),验证队列灵敏度43.3%、特异度90.0%(图5F)。单标志物分析显示,1-(环己基甲基)脯氨酸与N-十六酰基吡咯烷诊断效能最优,在发现队列AUC分别为0.693、0.782,在验证队列中AUC分别升至0.828、0.888,具备良好的独立诊断价值。
上述结果表明,肌少症患者存在显著的血浆代谢紊乱,核心以氨基酸代谢通路异常为特征;本研究构建的7 代谢物贝叶斯模型具有良好的诊断效能,1-(环己基甲基) 脯氨酸和N-十六酰基吡咯烷可作为肌少症潜在代谢生物标志物,为后续多组学整合诊断模型构建奠定了代谢组学基础。
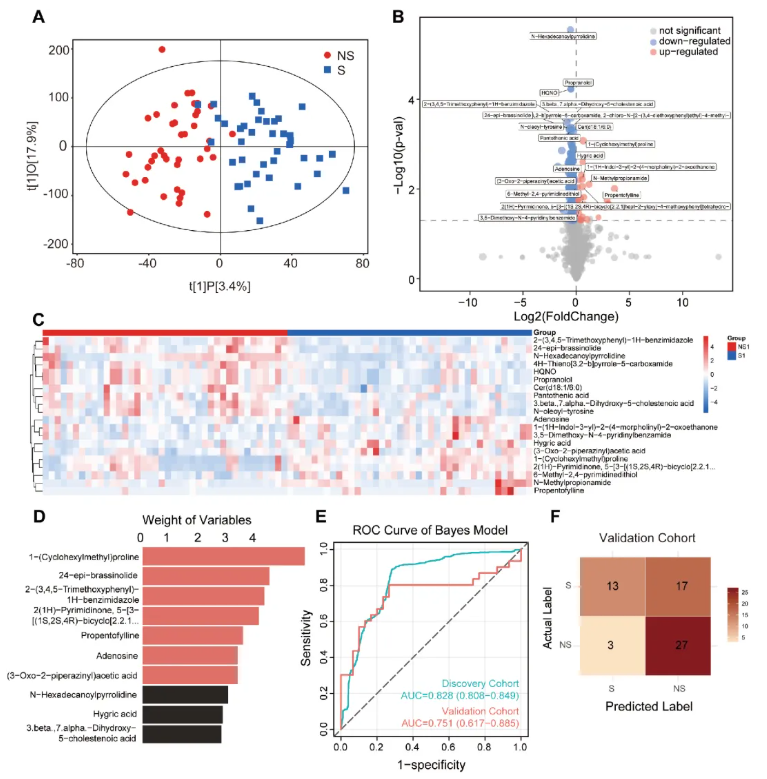
图5. 肌少症组与非肌少症组的代谢特征
04.多组学联合模型优于单组学方法
为提升肌少症诊断效能并增强临床适用性,本研究基于前期筛选的蛋白质组学和代谢组学最优模型及核心标志物,构建两种多组学联合诊断模型,对比其诊断性能并验证稳健性。结果显示,联合模型1整合7蛋白贝叶斯模型与7代谢物贝叶斯模型的概率输出,在发现队列AUC达0.951,显著优于单组学模型;验证队列AUC为0.823,显著优于蛋白质组学模型,与代谢组学模型无显著差异(图6A–C)。
联合模型2选取蛋白质组与代谢组各前2个最优标志物(CCL13、FGF2、1-(环己基甲基) 脯氨酸、N-十六酰基吡咯烷)构建;发现队列AUC为0.853,显著优于单组学模型;验证队列AUC为0.911,显著优于两个单组学模型,且与联合模型1验证效能相当(图6A–C)。该模型在验证队列中灵敏度86.7%、特异度80.0%、精确率81.2%、F1值0.839,整体诊断效能优异。
稳健性分析显示,将BMI作为协变量纳入联合模型2后,验证队列AUC为0.936;按年龄分层(<70岁vs≥70岁)后,AUC分别为0.924和0.883,不同年龄层间性能无显著差异。校准分析表明,联合模型2的预测概率与实际观测结果一致性更高(图6D);决策曲线分析(DCA)证实其临床净获益高于单组学模型(图6E)。研究进一步构建联合模型2列线图,可直观用于肌少症风险评估(图6F)。
综合表明,多组学整合模型诊断效能显著优于单组学模型;仅包含4个标志物的联合模型2兼具高诊断性能、良好稳健性与临床适用性,是肌少症血浆无创诊断的理想候选模型。
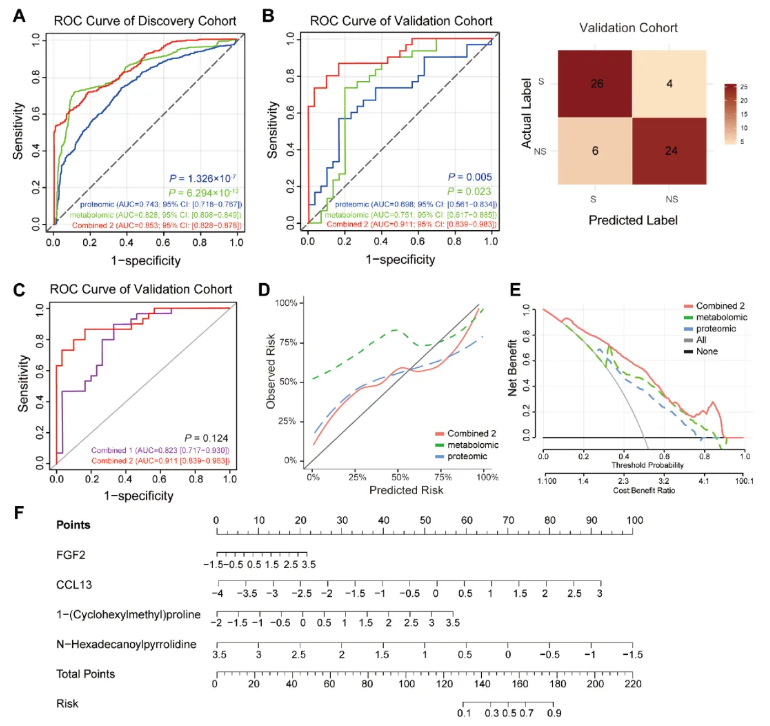
图6. 评估蛋白质组学、代谢组学模型及联合模型2对肌少症的预测能力
研究总结
本研究将Olink蛋白质组学和代谢组学整合到机器学习中,建立了基于血浆的高性能肌少症诊断模型。同时证明多组学整合方法显著优于单一组学方法,能更全面地反映疾病的复杂性。关键的是,研究发现了一个高效、精简的四生物标志物组合(CCL13、FGF2、N-十六酰基吡咯烷、1-(环己基甲基)脯氨酸),该组合因其精简特性展现出卓越的诊断准确性及强大的临床转化潜力。除诊断价值外,研究结果进一步证实炎症紊乱与代谢异常在肌少症发病机制中均起重要作用,为深入探索其机制及制定治疗策略提供了新见解。