
英文标题:Dynamic single-cell metabolomics reveals cell-cell interaction between tumor cells and macrophages
中文标题:动态单细胞代谢组学揭示肿瘤细胞与巨噬细胞之间的细胞相互作用
发表期刊:nature communications
影响因子:15.7
研究背景
代谢重编程是肿瘤发生发展的核心特征,肿瘤微环境中肿瘤细胞与巨噬细胞的代谢互作调控二者表型与功能,但其单细胞水平的动态代谢交流机制尚未明晰。传统代谢组学仅能静态检测代谢物浓度,无法反映代谢通路的真实活性;单细胞代谢分析与稳定同位素示踪技术的结合虽为解析单细胞代谢动态提供了可能,却受限于高通量检测技术短板与精准数据解析瓶颈,且常规共培养分析的分离或标记操作易干扰细胞天然代谢状态,难以精准解析二者直接的代谢互作,同时肿瘤相关巨噬细胞的极化异质性也缺乏基于代谢特征的单细胞分型方法。本研究构建高通量、无标记的单细胞动态代谢组学分析系统,结合稳定同位素示踪与机器学习技术,从静态浓度和动态活性双维度解析肿瘤细胞与巨噬细胞的直接代谢互作规律,揭示肿瘤微环境的代谢调控机制并实现肿瘤相关巨噬细胞的代谢特征精准分型。
研究结论
01.动态单细胞代谢组学系统的构建
研究人员基于适用于群体系统的MetTracer全局同位素示踪技术,构建了单细胞同位素示踪分析流程(图2a)。系统整体工作流程如图1所示:细胞经同位素示踪剂标记后,由高通量数据采集平台(如有机质谱流式设备)分析,再通过基于Python的数据处理平台完成单细胞基本代谢数据处理和同位素示踪分析,实现了单细胞水平代谢活性谱分析、交错代谢网络流向分析及细胞间相互作用研究。
关键数据处理步骤包括单细胞脉冲峰选择、特征峰确定、代谢物注释及峰强度提取。在该数据采集条件下,通过总离子流(TIC)变化和细胞标志物的提取离子流(EIC)可见,一个单细胞脉冲含3-6个质谱图(图2b),这与细胞体积有关,而代谢物差异可能源于细胞内浓度及鞘液提取效率。
对10个细胞脉冲中特征峰的最大强度保留时间分析显示,多数峰在细胞脉冲内两个相邻质谱图(间隔135ms)即r1和r2处达最大强度(图2c-d)。其中,m/z 80-500的峰倾向于在r1达峰,m/z 500-1000的峰更可能在r2达峰,这与不同大小分子的电迁移速率一致。
分别基于m/z 306.0760(谷胱甘肽)、m/z 804.5760(磷脂酰丝氨酸(37:0))及每个细胞脉冲最大强度提取的单细胞代谢物强度热图,呈现出显著不同的代谢谱(图2e),且通过两种不同分子量细胞标志物确定的代谢物比仅用一种更多(图2f)。
此外,计算每个检测峰的信号背景比(SBR),仅保留SBR>3且在所有细胞中出现频率>20%的峰作为细胞特征峰,为后续分析奠定基础。
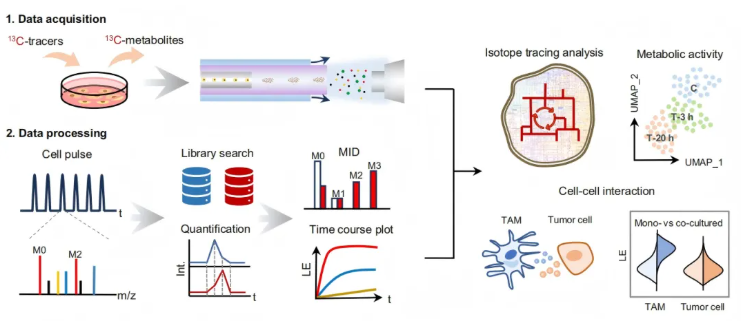
图1. 动态单细胞代谢组学系统的工作流程示意图
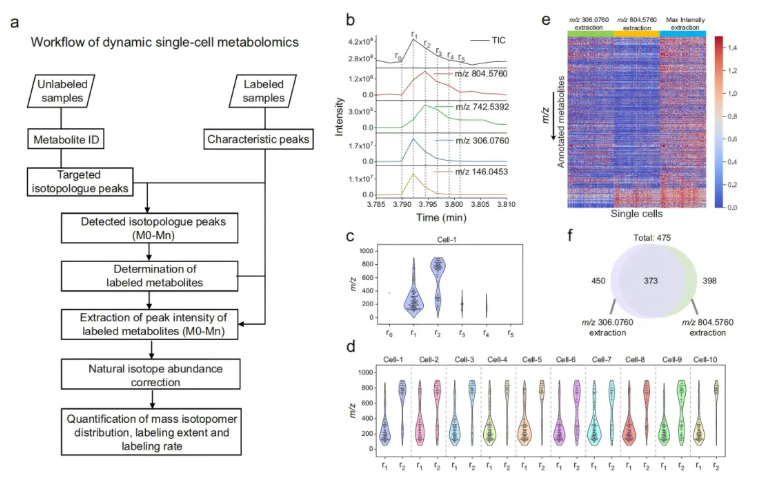
图2. 动态单细胞代谢组学数据处理平台
02.单细胞水平的全局代谢活性分析
为验证系统效果,研究人员以MDA-MB-231细胞为模型进行分析(图3a)。细胞在含透析胎牛血清(dFBS)的培养基中培养,分别用[U-¹³C]-葡萄糖和[U-¹³C]-谷氨酰胺标记5分钟至3小时,经优化后,3小时内共标记出40种代谢物(图3b)。KEGG富集分析显示,丙氨酸、天冬氨酸和谷氨酸代谢、精氨酸生物合成、三羧酸循环、嘌呤代谢等通路易被该方法标记和检测(图3c)。
在两种同位素标记条件下,标记代谢物被层次聚类为3个簇(图3d),并呈现出不同的时间进程模式:簇1的代谢物在3小时内达到同位素稳态,标记速率最高;簇2和簇3的代谢物3小时内未达稳态,标记速率依次降低(图3e-f)。通过非线性拟合计算各代谢物的标记速率(k),发现3个簇中代谢物的标记速率与时间进程模式一致(图3g-h),且这一结果在KEGG通路注释中得到验证(如葡萄糖标记下,半乳糖代谢和鞘脂代谢的标记速率较高;谷氨酰胺标记下,丙氨酸、天冬氨酸和谷氨酸代谢的标记速率较高,图3i-j)。
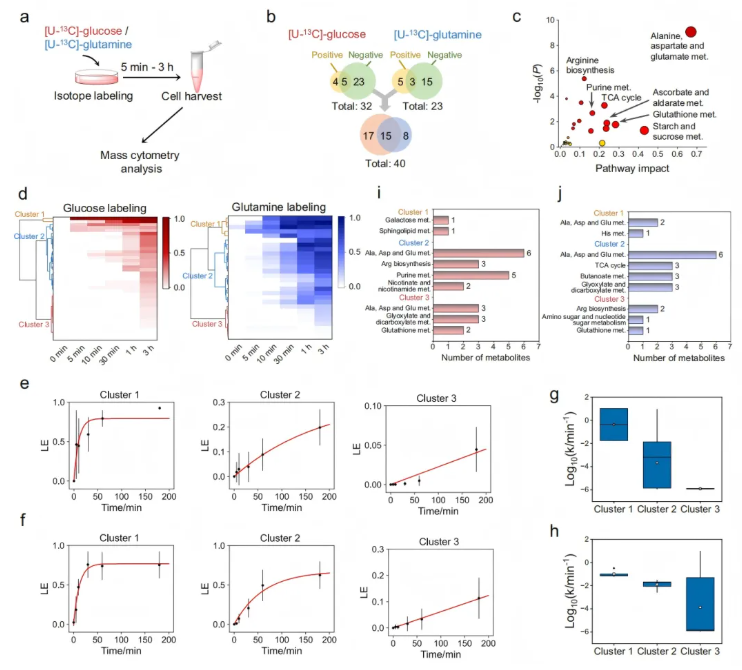
图3. 单细胞全局代谢活性分析
对约5000个经[U-¹³C]-葡萄糖标记的单细胞(涵盖6个标记时间点)进行分析,基于标记程度(LE)特征的UMAP分析识别出单细胞亚群(图4a)。通过密度聚类算法(DBSCAN)对所有细胞进行分析,得到A、B、C、D、E、F六个聚类(图4b),且各标记代谢物的LE从A到F依次升高,表明聚类A-F随标记时间呈演化趋势。不同时间组的单细胞在亚群中的分布存在差异(图4c),如5分钟、10分钟、30分钟、1小时和3小时组均包含多个亚群。这些结果揭示了代谢活动的异质性及单细胞在标记时间上的非同步性,这是传统批量分析无法捕捉的。
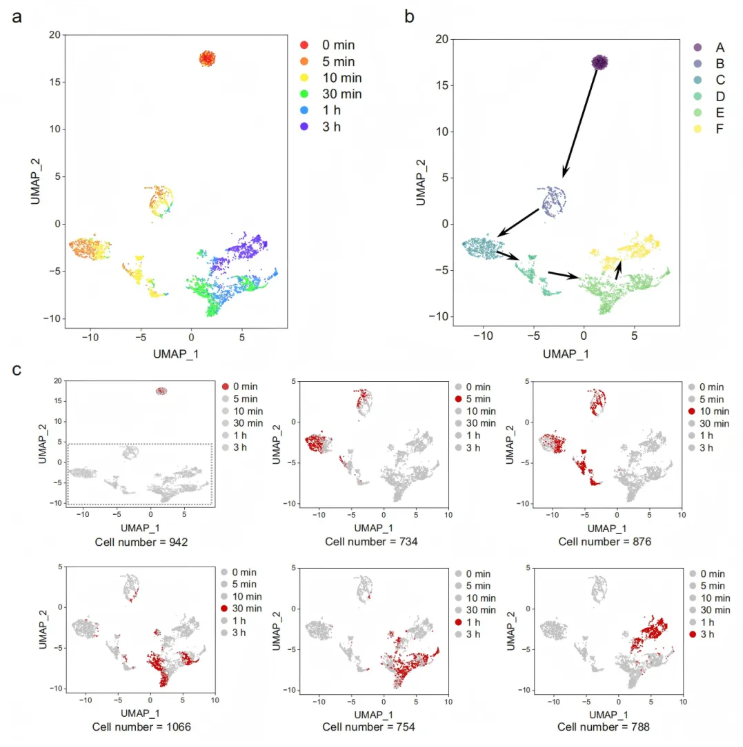
图4. 单个MDA-MB-231细胞代谢活性的细胞异质性
03.单细胞水平代谢途径的相互联系与流分析
以[U-¹³C]-葡萄糖为示踪剂,UDP-葡萄糖的M6同位素体显示其己糖部分通过糖酵解中间产物葡萄糖-1-磷酸在5分钟内快速标记(图5a);M5标记核糖经磷酸戊糖途径和嘧啶代谢生成,使UDP-葡萄糖的M11同位素体在1小时后出现,而M6标记程度在3小时后显著降低(图5b)。此外,三羧酸循环代谢物检测到多种标记同位素体(图5c),相关代谢物也呈现与循环阶段对应的标记模式(图5d)。
3小时标记样本的相关性矩阵分析揭示了单细胞通路间的关联(图5e-f)。仅用[U-¹³C]-乳酸示踪时,观察到M2标记的UDP-葡萄糖(图5g),且[U-¹³C]-乳酸未产生标记尿苷,表明其源于糖异生途径的己糖标记(图5h)。以[U-¹³C]-谷氨酰胺为示踪剂时,A549细胞中M3标记的苹果酸和天冬氨酸标记程度显著高于MDA-MB-231细胞,显示其还原活性更高(图5j)。
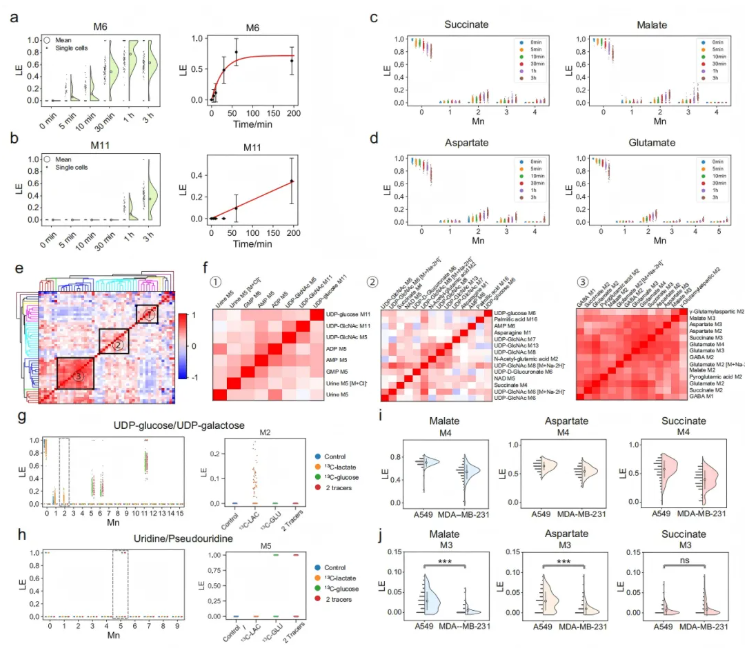
图5. 单细胞水平通过多种标记示踪剂揭示的代谢流及相互联系
04.2-脱氧葡萄糖诱导的单个MDA-MB-231细胞中的代谢扰动
研究人员比较了对照与2-脱氧葡萄糖(2-DG)处理条件下MDA-MB-231单细胞的代谢动态。2-DG通过抑制己糖激酶阻断糖酵解,生成2-DG-6P,处理组单细胞中可检测到该物质,且细胞形态和活力正常。
浓度分析显示,不同处理时间的2-DG组与对照组存在显著差异代谢物,涉及氨基糖代谢、嘌呤代谢等通路,部分代谢物(如PE、SM、谷氨酰胺)在3小时处理后浓度升高,可能是应对糖酵解抑制的早期机制。
动态分析中,UDP-葡萄糖/UDP-半乳糖的丰度无显著变化,但经[U-¹³C]-葡萄糖标记1小时后,其LE下降,表明糖酵解活性降低(图6a);UDP-GlcNAc的丰度在3小时处理后不变、过夜后降低,而其LE在两处理组均显著下降(图6b),且两种代谢物的标记速率在2-DG处理后降低(图6c-d),体现LE对短期代谢活性变化的灵敏反映。
层次聚类将标记代谢物分为两簇:簇1的LE降低,涉及糖酵解关联通路;簇2的LE升高,包括TCA循环等替代能量途径,且这些代谢物浓度均下调或无显著变化(图6e-f)。
降维分析显示,基于相对强度难以区分三组单细胞,结合LE可基于活性水平有效区分,而将代谢物相对强度与LE结合,区分效果更优(图6g-h),表明动态代谢组学是浓度分析的必要补充。
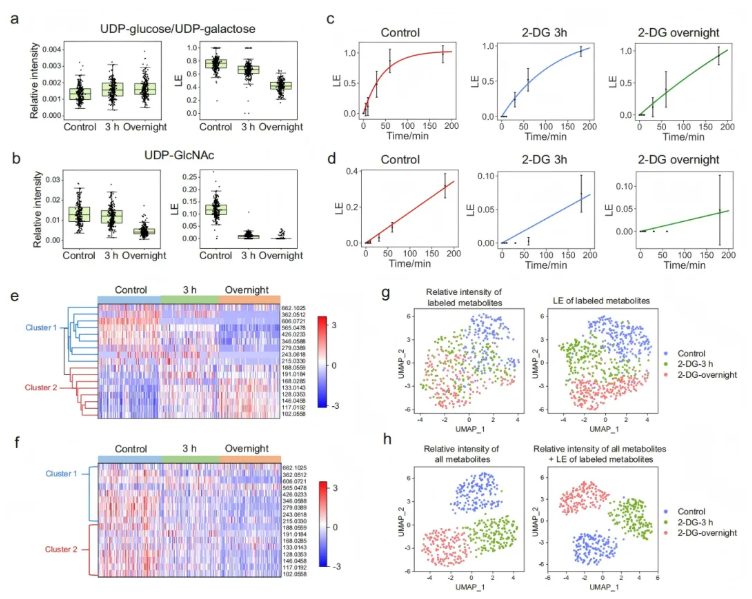
图6. 2-DG诱导的代谢活性扰动和单细胞聚类分析
05.肿瘤细胞与巨噬细胞之间的细胞相互作用
研究人员利用该系统分析MDA-MB-231肿瘤细胞与THP-1来源巨噬细胞的共培养体系,共培养细胞经UMAP分析分为两个簇(CD45⁺巨噬细胞与CD45⁻肿瘤细胞,图7a)。为精准分类细胞,开发了基于神经网络的监督机器学习模型(图7b),训练后验证准确率达 98.5%(图7c),能可靠区分两类细胞。
代谢活性分析显示,肿瘤相关巨噬细胞(TAM)与单独培养的巨噬细胞相比,氧化磷酸化、三羧酸循环等通路活性显著变化,且与浓度分析结果一致(图7g)。共培养的肿瘤细胞也呈现代谢适应性变化。
TAM中氧化磷酸化、三羧酸循环相关代谢物活性显著升高(图7h-i),而丰度无显著差异;UDP-GlcNAc丰度增加但代谢活性略降(图7j),提示其积累可能因消耗减少。
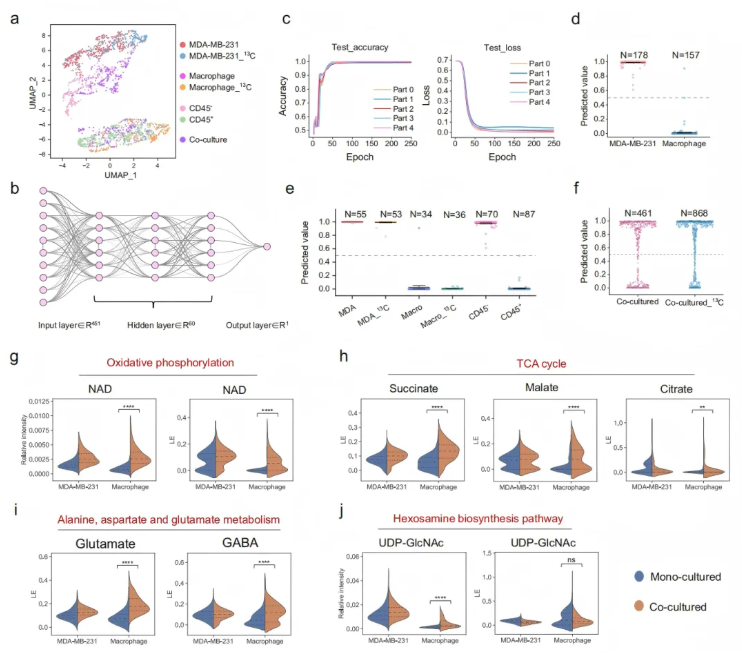
图7. 共培养的MDA-MB-231细胞与巨噬细胞的代谢组学分析
研究总结
本研究构建了结合同位素示踪与高通量分析的动态单细胞代谢组学系统,通过MDA-MB-231细胞代谢活性分析、代谢通路流解析、药物扰动验证及肿瘤-巨噬细胞互作研究,多维度证实其有效性。该系统突破传统批量分析局限,通过标记程度(LE)与浓度数据结合,实现从静态浓度到动态功能的解析,为细胞异质性研究、疾病模型构建及精准治疗提供了技术支撑与理论依据。
2026年2月9日,百趣生物首席科学家中国科学院上海有机化学研究所生物与化学交叉研究中心朱正江研究员及其团队在全球生命科学领域方法论研究顶级期刊nature methods(IF=32.1)发表题为“Deep-coverage single-cell metabolomics enabled by ion mobility-resolved mass cytometry”的研究论文。率先使用离子淌度质谱流式技术(ion mobility-resolved mass cytometry technology),创造性地结合高通量单细胞注射技术和离子淌度质谱,显著提升了单细胞代谢物检测的灵敏度、稳定性。