
代谢组学作为串联基因组、转录组、蛋白组与生物表型的关键纽带,其核心价值在于能直接捕捉生物体内小分子代谢物的动态变化,为癌症、自身免疫病等重大疾病的深层机制解析与治疗策略突破提供关键研究视角。百趣生物新一代代谢组学NGM,自推出以来持续为科研团队提供技术支撑——从代谢分子调控免疫细胞功能、驱动肿瘤进展,到解析微生物-宿主代谢互作,多个领域的关键研究成果已发表于影响因子(IF)>20的期刊,为疾病基础研究向临床转化奠定重要基础、注入潜在动能。以下将梳理部分前沿研究,直观展现代谢组学在不同疾病场景下的应用价值与创新潜力。
人类HDAC6介导缬氨酸感知,解锁DNA损伤与癌症治疗新方向

文章标题:Human HDAC6 senses valine abundancy to regulate DNA damage
发表期刊:nature
影响因子:48.5
本研究发现HDAC6通过其人源特有的SE14重复域可以直接与缬氨酸结合,且缬氨酸的缺乏会导致HDAC6在细胞核中的积累,进而诱导DNA损伤,其具体机制是核定位的HDAC6可以与TET2蛋白结合并对其去乙酰化,并对TET2的K1472、K1473、K1478位赖氨酸去乙酰化,从而激活DNA去甲基化过程,通过胸腺嘧啶DNA糖基化酶驱动的切除促进DNA损伤。此外,研究还验证了通过饮食限制缬氨酸可以抑制肿瘤生长,并增强PARP抑制剂的治疗效果。这一发现不仅揭示了缬氨酸在调控细胞DNA损伤与稳态中的新作用,还为癌症治疗提供了潜在的新策略。
肠道菌群代谢物丁酸——打破结直肠癌免疫治疗耐药壁垒
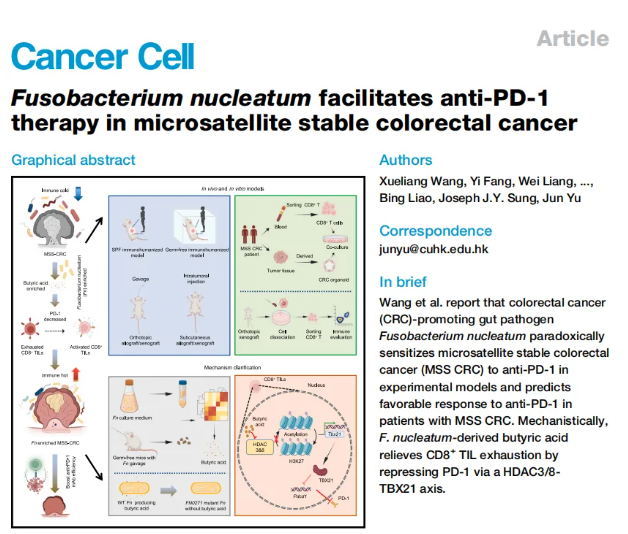
文章标题:Fusobacterium nucleatum facilitates anti-PD-1 therapy in microsatellite stable colorectal cancer
发表期刊:Cancer cell
影响因子:44.5
本研究借助代谢组学筛选与功能验证,揭示结直肠癌相关菌具核梭杆菌(Fn)的代谢产物丁酸,可成为微卫星稳定型结直肠癌(MSS CRC)免疫治疗的“增敏剂”:丁酸进入CD8⁺肿瘤浸润淋巴细胞(TILs)后,通过抑制HDAC3/8活性,增强Tbx21启动子H3K27乙酰化,上调转录因子TBX21并抑制PD-1表达,有效缓解CD8⁺TIL耗竭。临床数据显示,肿瘤内高Fn丰度与MSS CRC患者抗PD1治疗响应正相关;动物实验中,Fn灌胃或丁酸补充可显著提升抗PD1疗效,为MSS CRC这类“冷肿瘤”免疫治疗耐药提供微生物代谢解决方案。
VCP调控的代谢中间产物G3P——揭示肝细胞癌免疫抑制新通路

文章标题:VCP downstream metabolite glycerol-3-phosphate (G3P) inhibits CD8+T cells function in the HCC microenvironment
发表期刊:Signal Transduction and Targeted Therapy
影响因子:52.7
本研究揭示了VCP在HCC中通过稳定GPD1L(抑制其泛素化降解)促进G3P积累,进而通过直接结合CD8⁺T细胞中TCR信号通路关键激酶LCK(330-509位氨基酸)、增强其抑制性位点Tyr505磷酸化,阻断下游TCR信号(ZAP70、LAT、PI3K磷酸化降低),最终抑制CD8⁺T细胞活化及细胞毒性功能的新机制。临床层面,HCC患者肿瘤组织中VCP高表达与CD8⁺T细胞浸润减少、总生存期缩短显著相关,提示VCP可作为HCC不良预后生物标志物;动物实验证实,VCP抑制剂(CB-5083)或肝特异性敲除联合抗PD-1治疗,可显著提升CD8⁺T细胞浸润及细胞毒性,抑制肿瘤生长。研究结果不仅揭示了VCP作为HCC免疫抑制调控因子及预后标志物的双重重要作用,还为开发“VCP抑制剂+抗PD-1”的联合治疗方案提供了理论依据。未来的研究将进一步探索VCP-G3P轴在HCC临床转化中的应用,如基于VCP/GPD1L/G3P水平的患者分层、联合治疗的剂量优化及安全性评估。
丁酸调控免疫细胞——为自身免疫肝病治疗开辟新路径

文章标题:Gut Microbiota-Derived Butyrate Induces Epigenetic and Metabolic Reprogramming in Myeloid-Derived Suppressor Cells to Alleviate Primary Biliary Cholangitis
发表期刊:Gastroenterology
影响因子:25.1
基于代谢组学检测与临床样本关联分析,研究发现原发性胆汁性胆管炎(PBC)患者(尤其UDCA无应答者)粪便中丁酸水平显著降低,且与髓系来源抑制细胞(MDSCs)功能正相关。机制上,丁酸通过抑制HDAC3,增强MDSCs中PPARD及脂肪酸β-氧化(FAO)基因启动子的H3K27乙酰化,促进FAO驱动的线粒体氧化磷酸化(OXPHOS),进而诱导 MDSCs扩增并增强其抑制介导胆管损伤的自身反应性T细胞的能力。动物实验中,丁酸补充或丁酸产生菌灌胃可缓解免疫介导胆管炎;此外,丁酸还能修复PBC无应答者因FAO通路受损导致的MDSCs功能缺陷,为自身免疫肝病提供以肠道代谢为靶点的干预新思路。
菊粉-多形拟杆菌-十五烷酸轴:抑制NASH的新机制

文章标题:Parabacteroides distasonis uses dietary inulin to suppress NASH via its metabolite pentadecanoic acid
发表期刊:nature microbiology
影响因子:19.4
本研究聚焦非酒精性脂肪性肝炎(NASH)的饮食干预机制,发现可溶性膳食纤维菊粉可通过调控肠道菌群及代谢物抑制NASH进展。在胆碱缺乏高脂饮食(CDHFD)、高脂高胆固醇+ 高果糖(HFHCD)两种NASH小鼠模型中,菊粉较纤维素更显著缓解肝脏脂肪变性、炎症及纤维化,降低血清转氨酶(ALT/AST)、甘油三酯(TG)及促炎因子(TNF-α、IL-6)水平;借助¹³C-菊粉示踪与宏基因组测序证实,菊粉可富集肠道多形拟杆菌,该菌能利用菊粉合成十五烷酸,且菊粉、多形拟杆菌或十五烷酸可通过修复肠道屏障、下调肝脏炎症与脂质合成基因抑制NASH,为NASH肠道代谢干预提供新靶点。
这些研究虽聚焦不同疾病领域,却共同凸显了代谢组学在解析“代谢-疾病”复杂关联中的核心价值——从膳食成分、微生物代谢物到细胞内代谢中间产物,均可能通过精准调控分子通路成为疾病治疗的关键靶点。未来,百趣生物将继续深耕技术创新,助力更多生命科学问题的解答,推动领域持续突破!
告别同质化!百趣生物新一代代谢组学NGM 3现已重磅发布,助您精准突破科研瓶颈!