
文章标题:A Direct Infusion Probe for Rapid Metabolomics of Low-Volume Samples
发表期刊:Analytical Chemistry
影响因子:6.7
研究背景
代谢组学作为解析生物体系分子变化、挖掘生物样本代谢特征的重要手段,对样本量的需求持续向微量化发展,微量生物样本的高灵敏度、快速代谢组学分析成为领域内的关键研究与应用方向。直接输注质谱技术凭借分析速度快、检测覆盖广的优势,成为微量样本代谢组学分析的核心技术手段,然而现有直接输注检测探针普遍存在设计复杂、电离效率不足、微量样本检测重复性与稳定性欠佳等问题,难以适配微量样本的高效检测需求。针对这一技术痛点,相关研究团队设计开发了极简结构的直接输注探针(Direct Infusion Probe, DIP),通过系统优化探针工作参数,成功突破了微量样本代谢组学分析的技术瓶颈,为微量生物样本的快速、高灵敏度代谢组检测提供了全新的技术方案,也为微量代谢组学技术的发展与应用奠定了重要基础。
技术路线

研究结果
01.DIP的设计与优化
研究人员采用不锈钢毛细管结合PEEK样品三通接头搭建DIP核心结构,通过三通顶部通入氮气驱动文丘里自吸效应实现样本自主上样,同时在毛细管上直接施加高压完成气动辅助电喷雾电离,全面评估了探针结构设计对电离性能的影响(图1)。结果显示,该探针死体积仅0.14 μL,较传统纳升电喷雾源具备更优的溶剂脱溶效果,可实现微量样本从样品瓶到质谱进样口的快速转移与高效电离,为极微量样本的代谢组学检测提供了核心结构基础。
与此同时,研究人员对为探针-质谱距离、喷雾角度、氮气压力、电喷雾电压、质谱传输毛细管温度5项关键参数也进行了优化。优化后的DIP探针具备极简的结构设计、高效的电喷雾电离性能与优异的检测重复性,为极微量生物样本的快速代谢组学谱图分析提供了简便易用的核心工具。
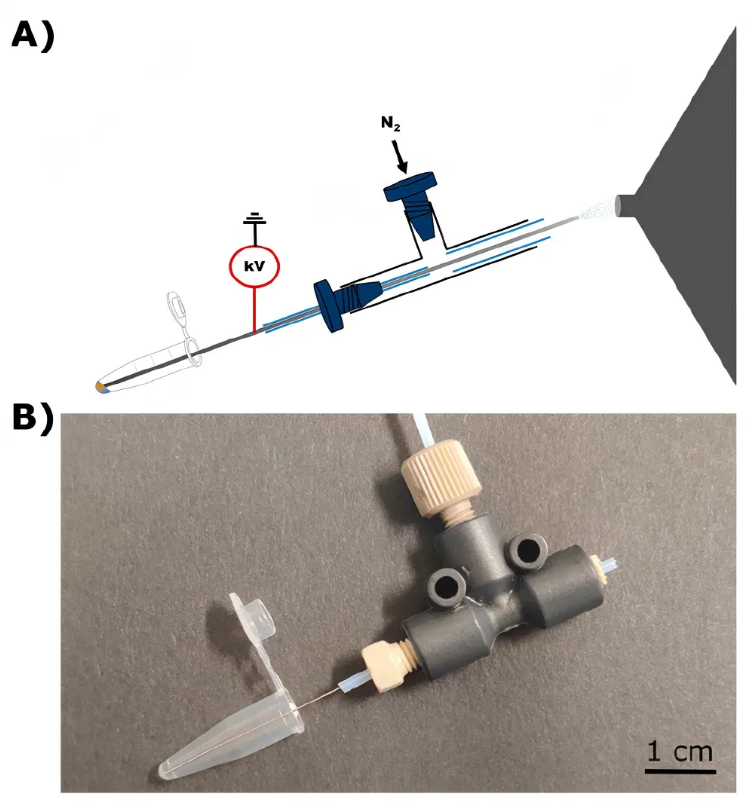
图1.直接输注探针(DIP)的设计
02.样本残留与检测重复性评估
为验证该方法下样本携带污染与检测重复性,研究人员通过交替进样含非内源性化合物的标准品溶液与大鼠脑组织内源性提取物溶液,测定DIP探针的样本间携带污染,同步通过提取离子流色谱图分析样本的信号轮廓特征(图2A)。结果显示,DIP探针仅需5 μL样本即可获得无纵向扩散的方波型信号轮廓,实现样本间的清晰分离;其毛细管体积仅0.14 μL,在1 μL/min流速下理论上仅需8秒即可完成管内溶液完全置换,连续进样10次扫描后样本平均携带污染仅2.5%,20次扫描后进一步降至1.1%,表明即使进样间不设置清洗步骤,DIP探针也具备极低的样本间携带污染,为高通量连续进样分析奠定了基础。与此同时,DIP探针同样具备合格的日间检测重复性,完全适配微量生物样本的快速、高通量代谢组学分析需求。
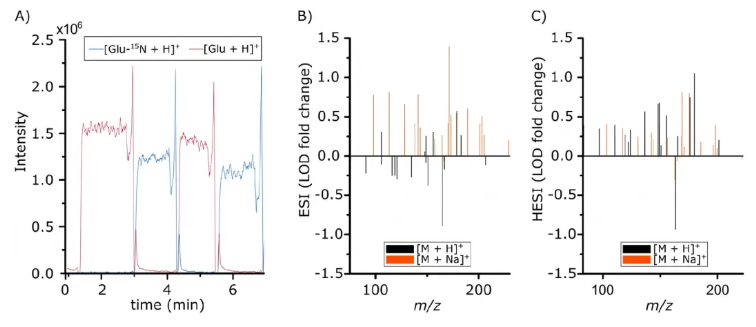
图2.样本残留率与商用电离源性能对比
03.与商用ESI离子源的性能对比
研究人员在同一台质谱仪上,分别采用DIP与商用ESI、HESI源,在各自优化的参数条件下检测25种具有生物学意义的代谢物与脂质标准品。结果显示,DIP的检测限(Limits Of Detection, LOD)相较于ESI和HESI源,平均分别优化了0.21倍和0.28倍;在检测到的47个标准品峰中,DIP分别有30个和42个峰的LOD优于ESI源与HESI源(图2B-C),表明尽管DIP设计极简、流速仅1 μL/min,其检测灵敏度仍与成熟的商用离子源完全相当。
为验证DIP对复杂生物样本的检测性能,研究人员采用大鼠脑组织提取物,评估了DIP对高盐复杂基质的耐受性与代谢物覆盖度(图3)。结果显示,DIP对高盐含量样本具有良好的耐受性,仅需单次无平均微扫描的质谱扫描,即可完成0.8 ng大鼠脑组织提取物的全面检测,覆盖从小极性代谢物到大分子疏水性脂质的广泛分子种类,包括20种氨基酸中的19种、神经递质、脂肪酸、甾醇、磷脂等物质;正离子模式下共初步注释到218个特征峰,其中120个为代谢物,证明仅使用极微量的生物样本,DIP仍能完整保留复杂样本的分子多样性。
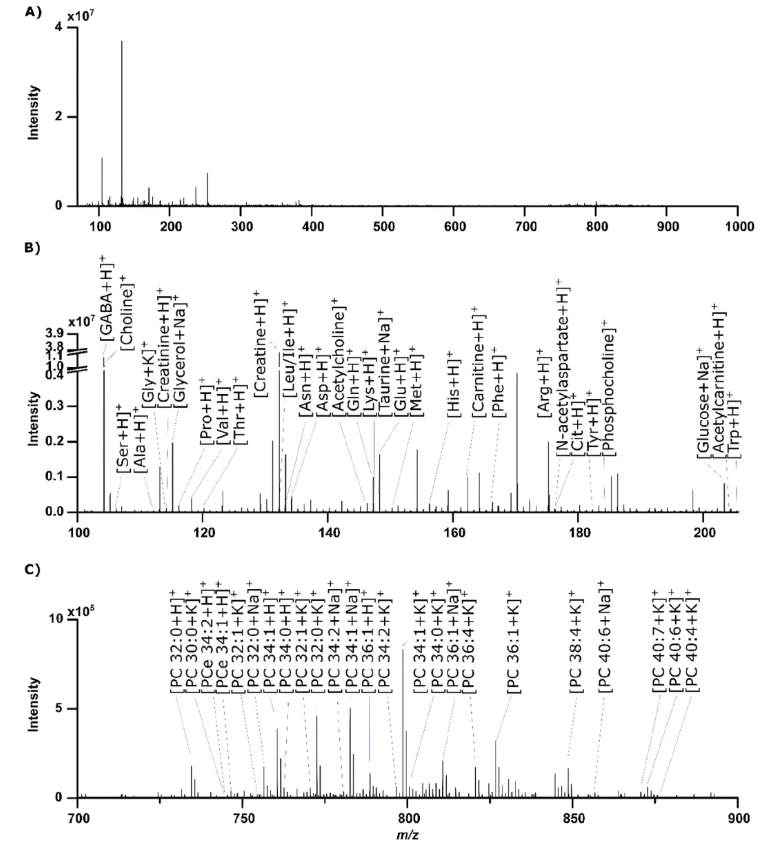
图3.采用DIP-MS分析,正离子模式下获得的单次扫描高分辨率光谱
04.低细胞数量样本中的代谢物检测能力验证
已知传统代谢组学分析需数十微升样本体积与至少百万级细胞量,难以实现荧光激活细胞分选(FACS)稀有样本、微量原代细胞等低细胞量标本的代谢谱分析,为系统验证DIP探针对低细胞数量样本的代谢物检测能力,明确微量细胞分析的性能边界。研究人员制备了细胞密度为20-500个细胞/μL的HEK293细胞甲醇提取物,取5 μL样本进行DIP-MS分析,通过稳定同位素内标对选定内源性分子进行定量检测。结果显示,代谢物检测信号强度随细胞密度升高呈递增趋势,即使细胞密度低至20个细胞/μL,仍可稳定获取氨基酸、葡萄糖等小分子代谢物与脂质的检测信息,最低可检测浓度达0.1 μM;定量结果显示HEK细胞内丰度最高的代谢物为谷氨酸,其次为天冬氨酸与丙氨酸,丰度最高的脂质磷脂酰胆碱PC 34:1浓度与葡萄糖水平相近,实现了微量细胞样本中代谢物与脂质的同步定量(图4)。
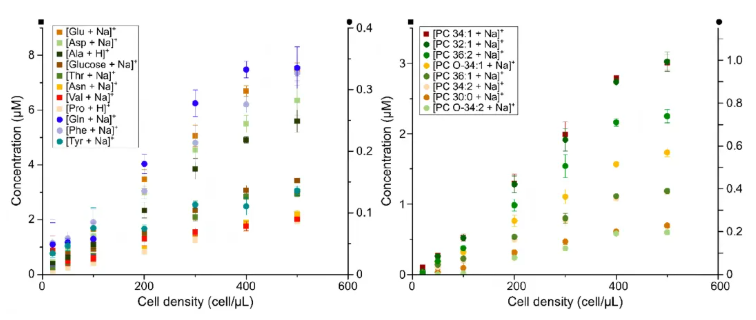
图4.低细胞密度样本中内源性代谢物与脂质的定量分析
05.葡萄糖刺激的INS-1细胞中的代谢物变化分析
已知胰岛素分泌型INS-1细胞是研究葡萄糖刺激胰岛素释放机制的经典模型,而现有代谢组学方法难以快速捕捉短时间葡萄糖刺激下的胞内瞬时代谢动态变化。为验证该方法的生物学应用价值,该研究采用DIP探针对高低葡萄糖刺激的INS-1细胞同步开展了非靶标与定量靶标代谢组学分析。
研究人员使用DIP探针,对分别暴露于1 mM(低糖)或20 mM(高糖)葡萄糖15分钟的INS-1细胞进行检测,基于精确质量完成代谢物初步注释,通过火山图展示组间差异代谢物,利用全局代谢网络图谱分析差异代谢物的通路关联(图5A-B)。结果显示,高糖刺激引发了细胞代谢组的显著动态变化,高糖组细胞中天冬氨酸水平下调0.4倍,多元醇通路特征产物山梨醇仅在高糖环境的细胞中被检出;差异代谢物显著富集于丙氨酸-天冬氨酸-谷氨酸代谢、精氨酸-脯氨酸代谢等氨基酸代谢通路,以及脂肪酸生物合成、甘油磷脂代谢、三羧酸循环等胰岛素分泌调控关键通路,负离子模式的重复实验也验证了一致的通路变化结果,表明DIP能够在短时间分析中,从少量细胞中获取与胞内代谢动态相关的有效生物学数据。
为进一步明确高糖刺激下的代谢物浓度变化,研究人员同步加入同位素标记内标,对目标代谢物开展靶标定量分析,对比高低糖组的代谢物水平差异(图5C)。结果显示,20 mM葡萄糖暴露可导致细胞内多种代谢物浓度发生统计学显著变化,除葡萄糖浓度升高外,谷氨酸、油酸(FA 18:1)、丙氨酸、GABA水平均显著上调,与葡萄糖代谢调控胰岛素分泌的经典机制高度契合。
综上数据,DIP探针可同步实现生物样本的非靶标代谢组谱图分析与精准靶标定量检测,能完整捕捉葡萄糖刺激下胰岛β细胞的代谢动态变化,为糖代谢机制研究与微量细胞的功能代谢分析提供了可靠的全新技术工具。
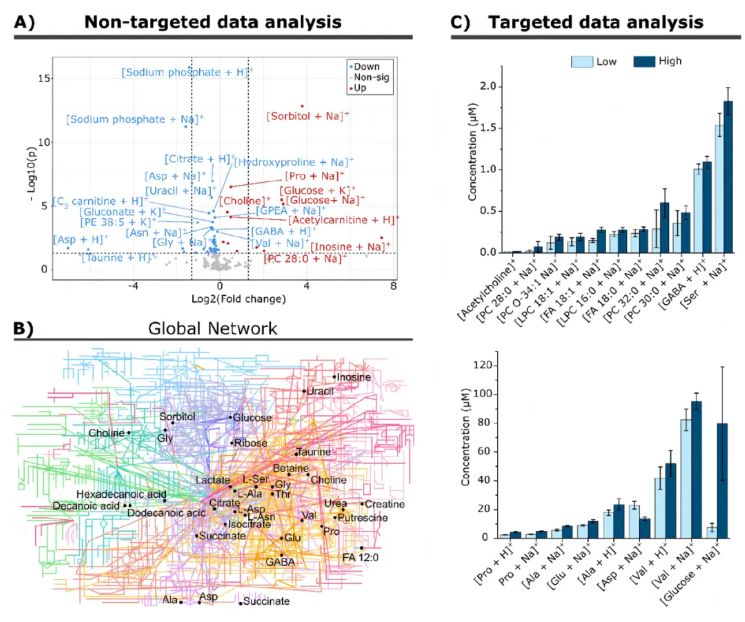
图5.INS-1细胞在低浓度/高浓度葡萄糖暴露下的非靶标及定量靶标代谢物谱分析
研究总结
该研究中,研究人员研发了一种用于直接输注质谱分析的探针——DIP,该探针结构简单、性能稳定,可对细胞、组织等化学组成复杂的生物样本实现快速分析。该探针仅需低至5 μL的样本体积、细胞密度低至20个细胞/μL的样本,即可获得数分钟的稳定检测数据。该技术为流式分选稀有细胞、微量原代细胞及各类小体积样本的高通量代谢组学研究开辟了全新可能。DIP探针对高盐负荷、不同浓度的复杂生物样本均具有良好的耐受性,且样本间携带污染极低,大幅减少了细胞/组织代谢物提取后繁琐耗时的样本前处理步骤,有望成为传统直接输注质谱技术在代谢谱分析领域的理想替代方案。
该技术可同步实现非靶标代谢谱分析与目标代谢物的靶标定量检测,从而对代谢组进行定性与定量双重表征。此外,极简的样本前处理流程与无需分子种类预筛选的特性,可同步获取覆盖多类代谢物与脂质的全面检测数据。